 圖/Shutterstock
圖/Shutterstock
公司介紹
MVC基亞疫苗科技股份有限公司於2012年10月正式成立,2014年5月初,公司更名為 基亞疫苗生物製劑股份有限公司,2017年6月7日更名為高端疫苗生物製劑股份有限公司。為一專注於細胞培養量產與疫苗開發而成立的研發型生技公司,擁有國內首座PIC/S GMP細胞培養疫苗量產廠。
高端為細胞培養技術之疫苗廠,具眾多優勢
細胞培養技術是現今生物醫藥產品中最重要的技術之一。高端疫苗主要的核心技術聚焦在「細胞培養」的製程優化與後續量產,新型的細胞培養技術是採用選定的細胞株代替傳統動物活體組織,作為病毒感染媒介並藉以量產疫苗。細胞培養製程的優勢主要有四項。1.封閉式生物反應器,透過一次性的生產系統與無血清培養基,大幅降低產品污染的風險2.細胞株與培養基儲備容易,不易有原物料短缺問題,使產量穩定、可靠3.生產時間較短,可快速進行製程放大4.製程應用性廣,有利於調節設備使用率,可達到單一產線生產多樣產品的運作優勢。
下圖為高端疫苗的R&D產品線

資料來源: 高端疫苗
一般新藥公司早期都是處於虧損的狀況,原因在於初期投入大量的金錢在研發新藥,而藥品開發前期不會有營收,但各項費用、成本、設備折舊等,常會造成公司大幅度虧損,因此需要仰賴股東或外界持續注資。在國外,當藥品越接近上市,成功機率越高,市場願意給的評價也越高,一旦成功研發新藥並取得專利,未來將帶給公司數十年之專利銷售、利潤。由於高端還處於研發前期,目前並沒有穩定的營收,目前預估最主要能為高端帶來營收之三樣產品,分別為新冠肺炎疫苗、腸病毒疫苗以及代理之四價流感疫苗。
高端疫苗為國產疫苗的最大受惠者:
新冠肺炎自2020年以來肆虐全球,即使疫苗逐漸問世,對中低收入國家,疫情依然不容小覷,近日印度單日確診屢屢突破30萬人,日本、泰國等亞洲國家疫情依然險峻,台灣近日接連爆出本土病例,華航群聚疫情也超過前次部桃群聚的規模,情況日益嚴重。
高端的候選疫苗MVC-COV1901技轉自美國國衛院(NIH)的基因重組S-2P棘蛋白技術,關鍵優勢為:更穩定、抗原的變異低(維持在pre-fusion form);更易誘發免疫反應、產生抗體,不會與宿主細胞融合,具更好的安全性,並於2020年12月開始新冠疫苗之一期測試,2021年3月30宣布完成疫苗二期收案,此計畫招募了超過4000位受試者,包含746位65歲以上受試者,亦在4月28日完成第二劑施打,目標在6月申請台灣緊急使用授權(EUA)。
為了達到台灣群體免疫,預估需要取得約4500萬劑疫苗,除了從國外進口約2000萬劑外,規劃其餘缺口2500萬劑,將以國內疫苗作為優先考量,政府目前評估將在2021下半年採購1000萬劑疫苗,在台灣流感疫苗大廠國光生技(4142)在新冠疫苗第一期臨床試驗效果不如預期,國內兩家疫苗廠商高端疫苗與聯亞生技(6562)預計各取得500萬劑,高端預計在2021年六月進行第二期臨床之解盲,在6月中下旬取得台灣緊急使用授權(EUA),並從7月開始分四到五次交付,目前高端疫苗已有200萬劑新冠疫苗之產能,第三季將達到500萬劑,第四季可望達到1000萬劑。
高端疫苗二期解盲結果已經於2021年6月10日公布,新冠肺炎疫苗期間分析數據顯示安全性與耐受性良好,所有受試者未出現疫苗相關嚴重不良反應。在免疫生成性部分,不區分年齡組情況下,疫苗組在施打第二劑後28天的血清陽轉率(seroconversion rate)達99.8%;中和抗體之幾何平均效價(GMT titer)為662,GMT倍率比值為163倍增加。而20~64歲之疫苗組,血清陽轉率則為99.9%,中和抗體幾何平均效價(GMT titer)為733,GMT倍率比值為180倍增加,將盡快送審EUA。
EUA主要評估標準為要有3000名受試者資料以確保疫苗安全性,國產疫苗受試者體內中和抗體效價不得低於接種AZ疫苗者,目前在安全性方面,除了在人數上符合標準,若從主觀的發燒來看,高端疫苗是很安全的,若和國外已經取得EUA的腺病毒、mRNA疫苗相比,全身性的不良事件頭痛、倦怠約是其他疫苗的三分之一;發燒機率小於0.7%,其他最接近的疫苗至少是十倍機率以上。與AZ疫苗的比較方面,比較保護力最大的困難是台灣中研院做的GMT數值,跟美國NIH的GMT值可能代表意義不一樣,因為用的方法、病毒不同,因此沒辦法就表面數字精準判斷,高端疫苗目前跟中研院、長庚大學正在努力把GMT值662倍轉換成國際共標,但也還得等上一段時間,因為要等到其他藥廠做相同步驟,報出他們的數字。所以最快方式還是免疫橋接(直接把AZ跟高端施打後放到同一個環境中,看看比較出來的結果,如果發現相關數據是差不多的,即證實高端疫苗的保護力相當於AZ疫苗)。我國疫情嚴重,且無法從外面得到充足的疫苗供給的情況下,高端疫苗有望通過台灣緊急授權使用,評估採購量將達到700萬劑。
以售價而言可參考高端曾與馬來西亞公司MGB (Metronic Global Bhd) 的醫療事業子公司MMSB (Metronic Medicare SdnBhd)簽署之疫苗採購備忘錄,以最高50美元、最多300萬劑進行協商,出廠價約為35美元,換算單劑疫苗大概是每劑1000新台幣,考量政府購買量大於300萬劑,可能有價格折讓,且第一批疫苗是提供台灣政府公費施打,因此售價可能略低於1000元,評估為850元。
考量高端疫苗的佐劑、預充針筒、玻璃瓶等都是外購,且目前各國外大廠都積極強購相關原料,因此研判相關成本將提高一倍左右,推估成本將略高於國外廠商,考量其售價較同源之莫德納疫苗高(30美金左右),因此預估毛利率將達55%。
高端2021上半年仍沒有產品可以貢獻營收,因此仍處於虧損的狀況,預計在六月中下旬,高端可通過EUA並正式開始履行與政府的500萬劑合約,反映到今年,預估主要的營收會落在第三季,並從7月就可以開始看到營收有顯著的成長,以台灣的取得疫苗的情況來看,高端疫苗非常有可能取得政府的疫苗500萬劑加購,這部分將搭配第四季高端提升的產能(第四季1000萬劑),因此第四季營收將與第三季相仿,但相關原料成本由於疫情嚴重,各疫苗大廠均在積極拉貨,包含針頭、佐劑等將會提高,因此毛利率較第三季稍差。
腸病毒71型疫苗解忙成功,邁向東南亞
腸病毒腸病毒在全球皆有分布,比起歐美等西方國家,腸病毒在亞洲(東南亞)更為盛行,對孩童造成的影響極大,可能造成腸胃不適、發燒甚至危及生命,且腸病毒之傳染力極強,過去曾在台灣、中國、東南亞肆虐,造成居民生命危險。
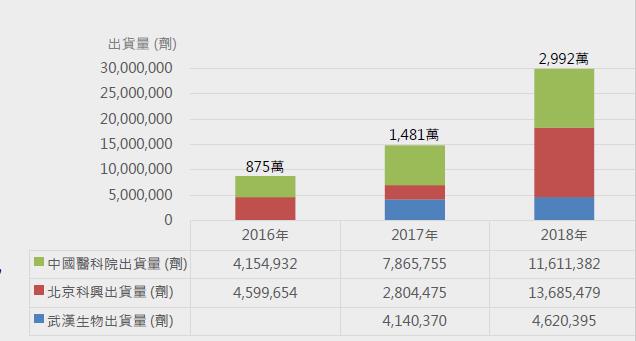
資料來源: 高端疫苗
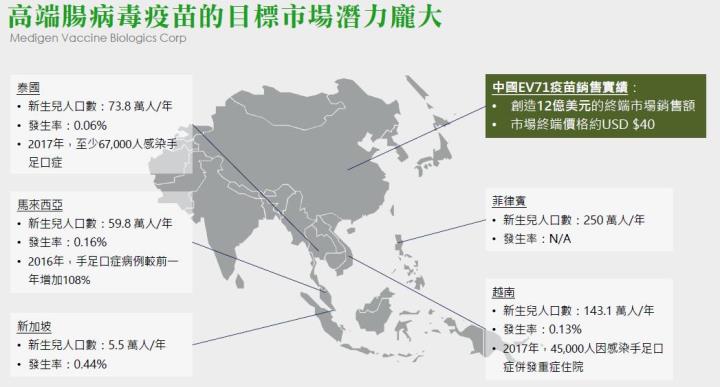 資料來源: 高端疫苗
資料來源: 高端疫苗
目前全球僅中國有三家廠商製造腸病毒疫苗,因無PIC/S GMP認證,市場侷限於中國,無法在世界其他地方銷售,而高端開發之腸病毒71型疫苗於2019年開始在台灣、越南進行測試,已在2021年4月宣布完成免疫生成性數據解盲,且數據達到台灣法規單位建議標準,完成臨床試驗報告後,將依加速核准機制,向衛福部食藥署申請新藥查驗登記、台灣上市許可,預估2022年可上市,以布局台灣為主,最終目標是打入目前人口仍處於高成長之東南亞國家,因此比起中國疫苗更有競爭力。
如同前述,高端疫苗的腸病毒疫苗技術為全球獨家,由上圖,我們可以看到腸病毒在東南亞國家造成的影響,也可以發現每年光是泰國、越南、新加坡、菲律賓及馬來西亞便有超過500萬名新生兒,在通過越南之臨床實驗後,高端不只可以在越南取得藥證進行銷售,更有望打入以東南亞國家為主的東協,因此看好未來主要市場在東南亞,預估高端年產能可達 300 到 500 萬劑,未來可能是支撐獲利的重要基礎。以中國廠商之價格作為參考,每劑腸病毒疫苗約為1000元新台幣,考量目前在台灣、越南之臨床實驗均成功,以已經測試過的越南、台灣兩地來推估,兩國一年之新生兒約有160萬人,疫苗可供6歲以下施打(一次兩劑),潛在市場高達1920萬劑,2022年銷售量預估將達到100萬劑(台灣為主),貢獻營收達10億。
代理流感疫苗,2021有機會貢獻營收
高端代理四價流感疫苗,產品來自韓國GC Pharma,目前已申請台灣許可證,預計2022 年有機會參與政府公費流感疫苗標案,以台灣每年公費流感600 萬劑(人)為計算基礎,隨著疫情升溫,上修50萬劑,加上自費施打每年約100萬劑,未來政府希望扶持國內疫苗廠商,因此預估疫苗的分配為國內與國外呈現七比三之水平,以每劑疫苗250元來算,高端可望出口100萬劑,貢獻營收2億5000萬元。
重要結論
一般新藥公司早期都是處於虧損的狀況,原因在於初期投入大量的金錢在研發新藥,而藥品開發前期不會有營收,但各項費用、成本、設備折舊等,常會造成公司大幅度虧損,因此需要仰賴股東或外界持續注資。在國外,當藥品越接近上市,成功機率越高,市場願意給的評價也越高,一旦成功研發新藥並取得專利,未來將帶給公司數十年之專利銷售、利潤。
目前高端疫苗有三種未來可望帶來獲利的產品。新冠疫苗已於2021/4/28完成第二劑施打,6月10日二期解盲成功,有望在2021年下半年開始施打,貢獻營收達59.5億元;中國腸病毒疫苗廠商,因無PIC/S GMP認證,市場侷限於中國,此外全球並無第二家有成功開發出腸病毒疫苗的廠商,而高端的腸病毒疫苗已於今年四月完成解盲,邁入申請藥證的階段,預估2022年開始貢獻營收,預估2022年達10億,東南亞市場為未來獲利的重要基礎;2022可望參加政府公費流感疫苗標案,預期將得到100萬劑之產量分配,貢獻營收達2億5000萬。
雖然高端疫苗屬於尚未穩定獲利之新藥公司,但新藥公司注重的是未來能否研發出新藥,目前疫情嚴重,市場投資人願意給予更高之市場信心,有望通過台灣緊急授權使用,因此給予逢低買進之評等,在正式通過EUA前,尚有向上的空間,但通過EUA後,投資人可能會更聚焦於三期試驗的進行,三期試驗需在國外進行,且成本高昂,如何取得資金來源,進行速度等都會有更多的疑問,市場相對震盪,在情況不變的情況下,加上第四季毛利率預期較第三季減少,股價高點可能出現在營收最旺的第三季。
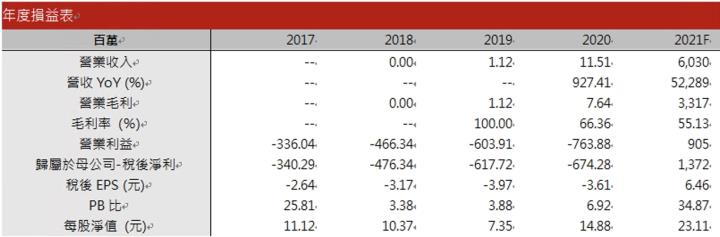
資料來源:CMoney

 發表
發表


 我的網誌
我的網誌


